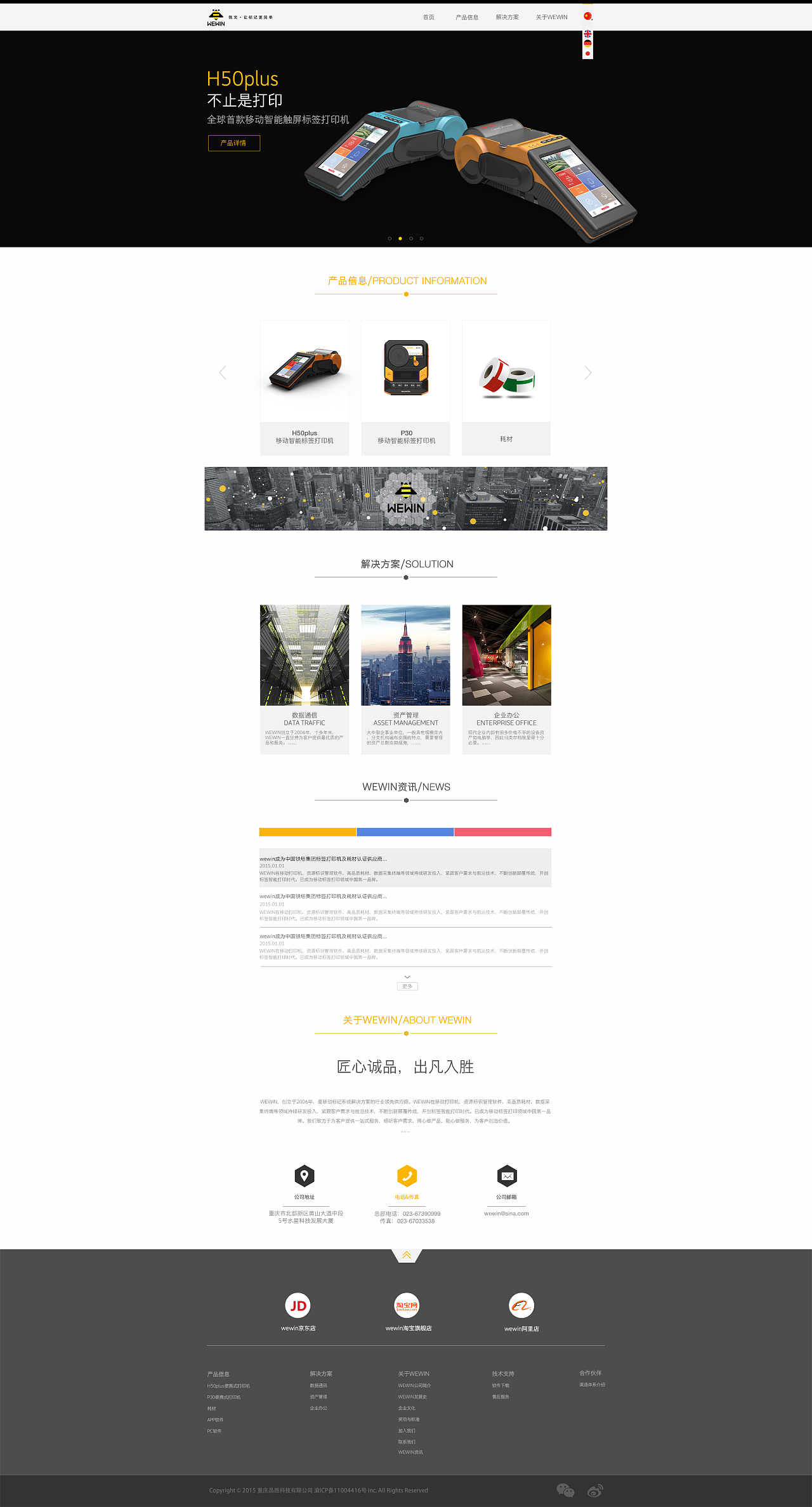
純凈空靈 產品網站設計的藝術與策略
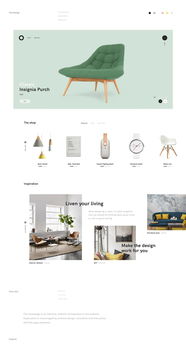
在當今數字化的時代,網站設計不僅僅是產品展示的平臺,更是品牌理念與用戶體驗的直接載體。'純凈空靈'的設計風格,以其簡約、透明和靈動的特質,正逐漸成為高端產品網站的首選。本文將探討如何實現這種設計風格,并分析其對用戶吸引力和轉化率的影響。
純凈空靈的設計核心在于'減法'。它摒棄了繁雜的視覺元素,強調留白與呼吸感。通過使用柔和的色彩調色板,如淺灰、純白和淡藍,設計師可以營造出一種寧靜而優雅的氛圍。例如,在蘋果公司的產品網站上,大面積的留白和簡潔的排版讓用戶的注意力集中在產品本身,增強了視覺沖擊力。這種設計不僅提升了美學價值,還減少了用戶的認知負荷,使他們能更快地理解產品核心信息。
空靈感往往通過動態元素和交互設計來體現。微妙的動畫效果,如淡入淡出、懸浮響應,可以賦予網站靈動的生命力。想象一下,一個產品圖片在滾動時輕微浮動,或按鈕以透明漸變的方式響應點擊,這些細節都能創造出一種輕盈、飄逸的體驗。研究表明,這種交互設計能顯著提升用戶的參與度和滿意度,因為它模擬了現實世界中的自然運動,讓用戶感覺網站是'活'的。
透明度的運用是'bon凈透空靈'風格的關鍵。設計師可以巧妙地使用半透明圖層或玻璃擬態效果,使內容與背景融為一體,又不失層次感。例如,在奢侈品或科技產品網站上,采用毛玻璃效果展示產品細節,能營造出神秘而高級的質感。同時,這種設計增強了網站的現代感,符合當前用戶對簡潔、高效界面的偏好。
實現純凈空靈的設計并非易事。它要求設計師在色彩、排版和動效之間找到平衡,避免過度簡化導致信息傳達不足。為此,建議采用用戶測試來迭代優化,確保設計既美觀又實用。從商業角度而言,這種風格能有效提升品牌形象,吸引追求品質的受眾,并最終提高轉化率。
純凈空靈的產品網站設計是一種以用戶為中心的藝術表達。它通過簡約的視覺語言和靈動的交互,創造出令人心曠神怡的在線體驗。隨著數字美學的發展,這種風格將繼續引領潮流,幫助品牌在競爭激烈的市場中脫穎而出。
如若轉載,請注明出處:http://www.fffnx.cn/product/14.html
更新時間:2026-04-18 14:36:58